ما المادة وكيف يمكن قياسها؟
المادة: هي كل شيء له كتلة وحجم
الكتلة: هي كمية الجسم تقاس الكتلة بوحدة الجرام ويستخدم الميزان لقياس الكتلة
الوزن: هو مقدار سحب الجاذبية للجسم ويقاص بوحدة النيوتن ويستخدم ميزان نابض
وزني على القمر أقل من وزني على الأرض لأن قوة جذب القمر لجسمي أقل من قوة جاذبية الأرض
الحجم: هو الحيز الذي يشغله الجسم
حجم الصلب: يقاس بالسنتمتر المكعب يساوي 3 سم
حجم السوائل: يقاس باللتر أو ملليتر

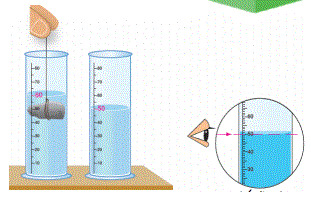
قياس حجم جسم صلب غير منتظم: يتم غمره بماء موضوع بمخبار مدرج ارتفاع الماء.
ونحسب التغير حيث أن مقدار ارتفاع الماء المزاح بالملليترات يشير إلى حجم الجسم
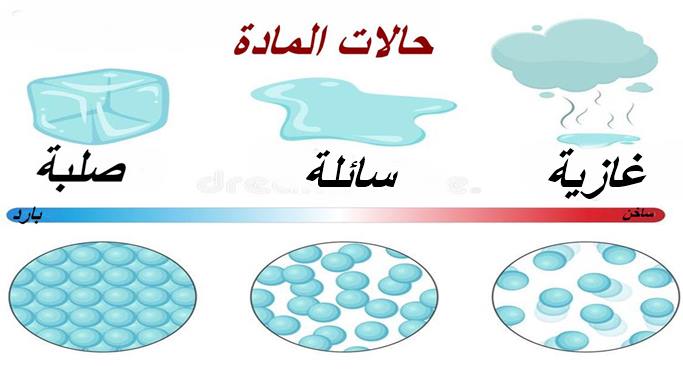
حالات المادة
1- حالة صلبة:
لها شكل ثابت، وتشغل حيز محدد وحركة جزيئاتها محدودة جدا وهي الحالة الأكثر كثافة للمادة
2- حالة سائلة:
ليس لها شكل محدد، وتأخذ شكل الوعاء الذي توضع فيه والجزيئات متوسطة التباعد وتزداد كثافة السائل عند تحوله للمادة الصلبة
3- الحالة الغازية:
ليس لها شكل محدد، تشغل أي حيز توضع فيه جزيئاتها في حركة مستمرة وتنتشر في كل مكان وهي الحالة الاقل كثافة للمادة
الكثافة:
مقدار الكتلة في حجم معين تقاس بالجرم لكل سنتمتر مكعب لكل مادة كثافة ويمكن حساب الكثافة بالقانون (الكثافة = الكتلة ÷ الحجم)
يطفو الجليد على الماء لأن كثافة الجليد
أقل أو يطفو الجسم عندما تكون كثافته
أقل من كثافة السائل
الطفو:
هو قدرة جسم على مقاومة الانغمار في مائع سائل أو غاز
تنشأ قوة الطفو لأن الجسم في أثناء الانغمار
يبعد المائع عن طريقه ليحل محله وفي الوقت
نفسه يدفع المائع الجسم إلى أعلى
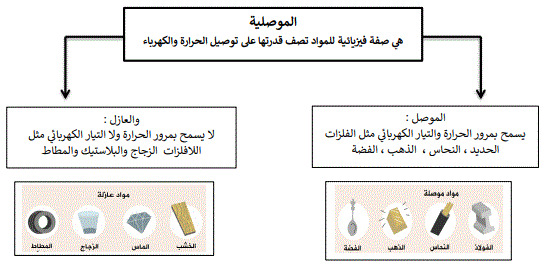
الخصائص الفيزيائية:
هي صفات يمكن ملاحظتها دون أن تغير في طبيعة المادة مثل الكثافة واللون والقساوة والمغناطيسية ودرجة الغليان والملمس
المخاليط
المخلوط:
مادتان أو أكثر تمتزجان معا ولا تكون مادة جديدة
مثال: السلطة التي تحتوي على طماطم وخيار وجزر وخس
المركب اتحاد عنصرين أو أكثر اتحادا كيميائيا
الحديد مع الكبريت مخلوط يمكن فصله بالمغناطيس
عند حدوث تفاعل كيميائي بين الحديد والكبريت ينتج مادة
جديدة تسمى كبريتيد الحديد
أنواع المخاليط:
المخاليط غير المتجانسة: يمكن تميز المواد بعضها عن بعض
مثل: الرمل مع الماء أو السلطة
المخاليط المتجانسة: لا يمكن تمييز المواد بعضها عن بعض مثل السكر مع الماء
المحلول خليط من مادة تذوب في مادة أخرى مثل: الملح والماء
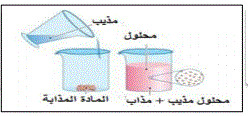
المذاب: هي المادة التي تذوب وكأنها اختفت مثل الملح - السكر
المذيب: هي المادة التي يذوب فيها المذاب مثل الماء
السبيكة: هي مخلوط مكون من فلز أو أكثر ممزوج مع مواد صلبة أخرى
السبائك محاليل
البرونز: يتكون من النحاس والقصدير
الذاتية: عند ذوبان السكر في الماء كلما أضفنا زيادة من السكر يصبح المحلول أحلى ونقول أنه ازداد تركيزه السكر وملح الطعام تزيد ذوبانها في المحلول عند زيادة درجة الحرارة
قانون حفظ الكتلة (الكتلة لا تفنى ولا تستحدث)
(هناك العديد من المخاليط المتجانسة وغير المتجانسة)
1- المعلق: مخلوط مكون من أجزاء ينفصل بعضها عن بعض مع مرور الوقت إذا ترك المخلوط ساكنا مثل: الرمل و الماء
2-- الغروي: مخلوط متجانس فيه دقائق مادة مشتتة خلال مادة أخرى, مسببة منع مرور الضوء من خلاله
3- المستحلب: مخلوط مكون من سائلين لا يذوبان ولا يمتزجان معا مثل: معجون الأسنان
(فصل المخاليط)
المغناطيسية: يفصل برادة الحديد عن المواد غير المغناطيسية
النخل: يفصل المنخل المواد ذات الحجوم المختلفة
الترشيح: يمكن استخدام مرشح لفصل الرمل عن الماء
التبخر: يتبخر الماء من محلول الماء المالح ويبقى الملح
التقطير: عملية تفصل فيها مكونات مخلوط بالتبخر والتكاثف يتم عمل التقطير عن طريق تسخين محلول من الملح الماء
والماء له درجة غليان من مخفضة وسيغلي أولا ويتحول إلى غاز ثم يتكاثف بخار الماء ويتم تجميعه في دورق آخر



