عرض بوربوينت التغيرات الكيميائية علوم سادس ابتدائي ف3
ما التغيرات الكيميائية
الأهداف التعليمية ومخرجات التعلم
1- وصف ثلاثة أنواع من التفاعلات الكيميائية.
2-مقارنة التفاعل الطارد للطاقة والتفاعل الماص لها
أن التغيرات الفيزيائية لا ينتج عنها مواد جديدة.
فكيف تتكون المواد الجديدة إذن؟
تتكون المواد من ذرات مرتبطة معا. عندما ترتبط ذرات مع ذرات أخرى تتكوَّن الرابطة الكيميائيَّة.
الرابطة الكيميائية
قوة تجعل الذرات تترابط معاً , تكوين هذه الروابط أو تفكيكها يغير الخصائص الكيميائية للمادة
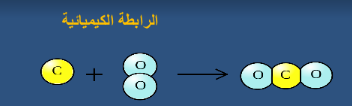
مادة الفحم تتكون من ذرات الكربون المترابطة
عندما يحترق الفحم فإن جزيئات الأكسجين في الهواء تترابط مع ذرات الكربون مكونة جزيئات جديدة من ثاني أكسيد الكربون الذي يختلف في خصائصه عن كل من الكربون والأكسجين
التغير الكيميائي
تغير ينتج عنه مواد جديدة لها خصائص كيميائية تختلف عن خصائص المواد الأصلية
التغير الكيميائي يمكن ملاحظة بعض العلامات التي قد تدل على حدوث التغير الكيميائي ( تغير اللون – تصاعد الغازات – انطلاق الحرارة أو الضوء )
بعض هذه العلامات قد تظهر دون حدوث تغير كيميائي
ومن ذلك تغير لون الماء عند إضافة ملونات الطعام.
وتغير اللون في هذه الحالة لا يدلُّ على حدوث تغير كيميائي لأنَّ ملون الطعام والماء خليط، ويمكن أن ينفصل أحدهما عن الآخر بالتبخُّر أو التقطير.
وصف التغيرات الكيميائية
التغيرات الكيميائية جزء من حياتنا اليومية
تغير أوراق الشجر , قلي البيض , خبز العجين , هضم الطعام , جميعها تغيرات كيميائية
وصف التغيرات الكيميائية
يتكون التفاعل الكيميائي من جزأين
مواد موجودة قبل حدوث التغير الكيميائي هي المواد المتفاعلة
ومواد تنتج عن التغير الكيميائي تسمى المواد الناتجة
وصف التغيرات الكيميائية

يوصف التفاعل الكيميائي بصورة رمزية باستخدام المعادلة الكيميائية
تستعمل المعادلة الكيميائية حروف وأرقام تدل على كميات المواد المتفاعلة والمواد الناتجة
يفصل السهم بين المواد المتفاعلة جهة ذيل السهم والمواد الناتجة جهة رأس السهم
وصف التغيرات الكيميائية

تتكون المواد المتفاعلة والمواد الناتجة من ذرات العناصر نفسها ولكن أعيد ترتيبها وطريقة ترابطها هناك أعداد ذرات متساوية لكل عنصر على جانبي السهم وهذا يعني أنَّ المعادلة الكيميائية موزونة يطلق العلماء على هذا قانون حفظ الكتلة.
وبناء على هذا القانون فإنَّ المادة لا تفنى ولا تستحدث وإنَّما تتحوَّل من شكل إلى آخر
فجميع الذرات الموجودة قبل التفاعل هي نفسها موجودة بعد انتهاء التفاعل
التفاعلات الكيميائية

هناك ثلاث أنواع من التفاعلات الكيميائية
1- تفاعل الاتحاد
ترتبط عناصر أو مركبات معاً لتكوين مركبات جديدة أكثر تعقيداً
التفاعل الذي يستخدم في الصناعة لإنتاج المواد الكيميائية عامة .
تتحد ذرات الحديد مع جزيئات الاكسجين لإنتاج اكسيد الحديد ( الصدأ )
2- التحلل الكيميائي

وهو عكس تفاعل الاتحاد الكيميائي تتفكك مركبات معقدة إلى مواد أبسط منها
عندما تحلِّل الخلايا أجزاء الطعام فإنَّها تقوم بتفاعل تحلّل كيميائي
فقاقيع المشروبات الغازية هي مواد ناتجة عن تفاعلات تحلل
3- تفاعل الإحلال
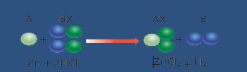
تتبادل العناصر الجزيئات أماكنها حيث يحل أحد العناصر محل آخر مكوناً مركباً جديداً
مثل : تفاعل حمض الهيدروكلوريك مع هيدروكسيد الصوديوم لتكوين الماء وكلوريد الصوديوم ( ملح الطعام )
يحل الخارصين محل الهيدروجين في مركب حمض الهيدروكلويك لتكوين كلوريد الخارصين و غاز الهيدروجين
سرعة التفاعلات الكيميائية
تعتمد سرعة التفاعل الكيميائي على عدة عوامل من أهمها
1- درجة الحرارة : فزيادة درجة الحرارة تسبب زيادة سرعة حركة الجزيئات.
2- التركيز : إنَّ زيادة التركيز أي زيادة كمية المواد المتفاعلة في المحلول تعني زيادة احتمال اتصال الجزيئات معا لتشكل الروابط الكيميائية
3- الضغط : زيادة الضغط تجبر أكبر عدد من الجزيئات على التجمُّع في مساحة صغيرة،
التفاعلات الماصة للطاقة والتفاعلات الطاردة للطاقة
إن المشعل ينْتج ضوءا وكمية من الحرارة كافية لقطع الفلز ينتج شعاع المشعل عن تفاعل غازين معا.
والغازان محفوظان في صهاريج قريبة ويتفاعلان معا بشدَّة، يعطي التفاعل بينهما الكثير من الطاقة في صورة ضوء وحرارة في مدة زمنيَّة قصيرة.
وهذا النوع من التفاعلات التي تطلق الطاقة يسمَّى التفاعلات الطاردة للطاقة
التفاعل الطارد للطاقة :
تفاعلات كيميائية تطلق طاقة
تستمر هذه التفاعلات في إطلاق الطاقة من لحظة بدئها حتى تتوقف
مثال : حرارة وضوء المشعل الكهربائي الذي يستخدم في اللحام / احتراق الشمعة ينتج طاقة حرارية وضوئية
التفاعلات الماصَّة للطاقة
هناك تفاعلات تحتاج إلى مصدر طاقة تسمَّى التفاعلات الماصَّة للطاقة.
تتطلَّب التفاعلات الماصة للطاقة توافر مصدر طاقة مستمر ليستمرَّ التفاعل.
إذا توقَّف هذا المصدر عن تزويد التفاعل بالطاقة فإنَّ التفاعل يتوقَّف فورا
عملية البناء الضوئي في النباتات مثال على التفاعلات الماصَّة للحرارة وهي لا تحدث دون تزويدها بطاقة من مصدر ضوئي
تقويم
نوع السؤال: صواب أم خطأ
1- المعادلة الكيميائية التالية تمثل تفاعل طارد للطاقة: حرارة + 4Fe + 3o3 → 2FeO3
أ- صواب
ب- خطأ
2- نوع التفاعل في المعادلة الكيمائية التالية: C + O → Co2
أ- اتحاد.
ب- تحلل.
ج- إحلال.
د- تعادل.
السؤال : كيف تتغير المادة كيميائيا
الجواب :
السؤال : المفردات. المواد التي تنتج عن التغير الكيميائي تُسمى
الجواب :
السؤال : ما بعض الدلائل التي تشير إلى التغير الكيميائي
الجواب :
السؤال : في المعادلة الكيميائية، ماذا يظهر جهة ذيل السهم وجهة رأس السهم؟
الجواب :
السؤال : إذا كانت المواد المتفاعلة في التغير الكيميائي تحتوي على ثلاثة عناصر، فماذا يمكن أن تتوقع للمواد الناتجة؟
الجواب :
السؤال: أختار الإجابة الصحيحة. أيّ مما يأتي ليس تغيرا كيميائيا
أ- احتراق الخشب.
ب- تحوّل لون شريحة التفاح إلى البني عند تعرضها للهواء.
ج- تصبح رائحة البيض الكريهة عندما يفسد.
د- اختلاط السكر بالماء.
السؤال: اختار الإجابة الصحيحة. أيّ مما يأتي مثال على تفاعلات التحلل؟
أ- تفاعل الحديد والأكسجين لتكوين أكسيد الحديد.
ب- تفاعل كلوريد الفضة والرصاص لتكوين كلوريد الرصاص والفضة.
ج- تكوّن ثاني أكسيد الكربون والماء من حمض الكربونيك.



